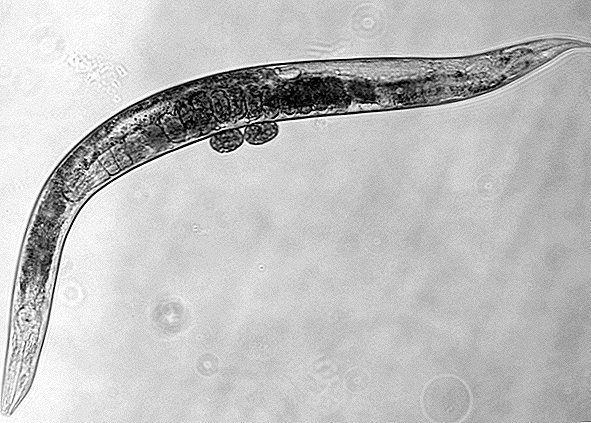
Durch die Optimierung einiger Schlüsselgene in der DNA eines Spulwurms haben Wissenschaftler die Lebensdauer des Tieres um etwa 500% verlängert.
Das ist ein großer Sprung ins Leben: Ein durchschnittlicher Spulwurm lebt etwa drei bis vier Wochen. Ohne zwei spezifische Gene - DAF-2 und RSKS-1 - können die Kreaturen mehrere Monate überleben.
Wissenschaftler hatten diese Gene vor Jahren mit der Langlebigkeit in Verbindung gebracht und festgestellt, dass sich die Lebensdauer von Würmern und anderen Lebewesen verlängert, wenn diese Gene ausgeschaltet werden. Die genaue Rolle der Gene im Alterungsprozess blieb jedoch ein Rätsel.
Jetzt haben Forscher die Punkte zwischen diesen beiden Genen und den Mitochondrien, den winzigen Kraftwerken, die die Brennstoffzellenfunktion im gesamten Körper erfüllen, miteinander verbunden. Mitochondrien beginnen mit zunehmendem Alter des Organismus zu versagen, aber die Stummschaltung von DAF-2 und RSKS-1 scheint diesen Schaden zu verzögern und die Lebensdauer zu verlängern - zumindest bei Spulwürmern, so eine Studie, die 2019 in der Zeitschrift Cell Press veröffentlicht wurde.
Nur die Zeit wird zeigen, ob das Anti-Aging-Mittel bei Säugetieren, einschließlich Menschen, wirken kann.
Domino-Effekt
Die Wissenschaftler erkannten den Zusammenhang zwischen DAF-2 und Alterung zum ersten Mal in den frühen neunziger Jahren, als ein Forscherteam entdeckte, dass Spulwürmer doppelt so lange leben wie normal, wenn sie eine mutierte Version des Gens tragen. Das Ergebnis leitete eine neue Ära in der Erforschung des Alterns ein, die von Genen und ihren Nebenprodukten angetrieben wurde.
"Es war wie ein Wegbereiter auf diesem Gebiet ... weil die Leute anfingen zu glauben, dass ein einziges Gen die Lebensdauer verlängern kann", sagte Co-Autor Pankaj Kapahi, Professor am Buck-Institut für Altersforschung in Novato, Kalifornien, gegenüber Live Science .
Im Laufe der Zeit entdeckten Forschungsgruppen mehr Langlebigkeitsgene, einschließlich RSKS-1, aber zunehmende Beweise deuteten darauf hin, dass diese speziellen Segmente des genetischen Codes nicht isoliert funktionieren. Stattdessen koordinieren sie sich mit einem Team anderer Gene und den Proteinen, die sie aufbauen, und lösen Kaskaden zellulärer Aktivität aus, die als "Signalwege" bekannt sind. Stellen Sie sich Signalwege als Reihen von Dominosteinen vor - wenn ein Dominostein umkippt, fällt er in einen anderen und löst eine komplizierte Kettenreaktion aus.
DAF-2 und RSKS-1 befinden sich jeweils in einem wichtigen Signalweg: dem Insulinsignalweg, der zur Kontrolle des Blutzuckerspiegels und des Stoffwechsels beiträgt, und dem TOR-Weg, der die Art und Weise verändert, wie Zellen Proteine aufbauen und somit wachsen und sich vermehren. Aber wie sich diese Wege in einem alternden Organismus kreuzen, sei nicht bekannt, sagte Kapahi.
Um herauszufinden, woher dieser Anti-Aging-Effekt kommt, haben Kapahi und seine Kollegen die Zellen mutierter Spulwürmer ausspioniert, in denen beide Gene ausgeschaltet waren. Mithilfe einer Technik namens "Polysomal Profiling" konnte das Team verfolgen, welche Proteine die Zellen zu einem bestimmten Zeitpunkt aufbauten. Während der Proteinkonstruktion können Zellen verschiedene Mechanismen einsetzen, um die Produktion eines bestimmten Proteins anzukurbeln oder es zurückzurufen. Das Team stellte fest, dass Zellen in mutierten Würmern weit weniger Kopien eines Proteins namens "Cytochrom c" bauten als normale Würmer.
Hier kommen Mitochondrien ins Spiel:
Cytochrom c erscheint in der inneren Membran der Mitochondrien und hilft dabei, negativ geladene Elektronen durch seine Struktur zu leiten. Dieser Elektronentransfer von Protein zu Protein ermöglicht es den Mitochondrien, Kraftstoff zu erzeugen. Bei mutierten Würmern tritt jedoch eine Lücke auf, in der sich Cytochrom c befinden sollte. Die Mitochondrien sind nicht in der Lage, Kraftstoff so effizient wie gewöhnlich herzustellen. Sie stellen die Energieerzeugung zurück und konzentrieren sich stattdessen auf die Reparatur beschädigter Gewebe.
Wenn die Energiespeicher sinken, schaltet ein Kraftstoffsensorenzym namens AMPK einen hohen Gang ein und hilft dem Wurm, auf eine effizientere Form des Energiestoffwechsels umzuschalten. Diese komplexe Kette von Ereignissen erzeugt letztendlich einen langlebigen Spulwurm, dessen Zellen bis ins hohe Alter gesund und weitgehend schadensfrei bleiben.
"Proteine werden mit zunehmendem Alter beschädigt, und Sie sehen weniger Schäden, wenn diese Wege gehemmt werden", sagte Kapahi. Untersuchungen deuten außerdem darauf hin, dass bestimmte Gewebe, wie z. B. Muskeln und Gehirn, möglicherweise sogar gesünder werden, solange diese Wege erstickt bleiben, fügte er hinzu.
Von Würmern zu Menschen
Insgesamt wählten die mutierten Würmer sowohl die Protein- als auch die Energieproduktion zurück, um ihre alternden Zellen zu reparieren. Insbesondere ein Mangel an Cytochrom c in den Fortpflanzungszellen der Tiere schien der Schlüssel zu diesem Prozess zu sein, stellten die Autoren fest. Es könnte sein, dass die Würmer Prozesse im Zusammenhang mit der Reproduktion im Energiesparmodus auf Eis legen, sagten sie.
Organismen reagieren ähnlich, wenn sie in den Hungermodus versetzt werden - ohne ausreichende Ernährung fordern zelluläre Signale den Körper auf, sich eine "Auszeit" von der Vorbereitung auf die Produktion von Nachkommen zu nehmen, sagte Kapahi. Diese Idee wird auch durch die Studie über Spulwürmer aus den 90er Jahren gestützt. In dieser Studie lebten die mutierten Würmer doppelt so lange wie normale Würmer, produzierten aber auch etwa 20% weniger Nachkommen.
Das Altern im Spulwurm ist kein passiver Prozess, sondern scheint ein chaotisches Gewirr biologischer Pfade zu beinhalten, die zusammenarbeiten, um den Stoffwechsel, die Proteinkonstruktion und möglicherweise die Reproduktion zu regulieren. Obwohl es beim Menschen ähnliche Wege gibt, wissen die Wissenschaftler immer noch nicht, ob das Altern bei beiden Organismen gleich funktioniert, sagte Kapahi. Wenn überhaupt, kann sich das Altern beim Menschen als komplexer erweisen.
"Die Erhaltung ist nicht absolut und es gibt wichtige Unterschiede zwischen Würmern und Säugetieren auf diesen Wegen", sagte Dr. Joseph Avruch, Professor für Medizin an der Harvard Medical School und Leiter der Diabetesabteilung am Massachusetts General Hospital, Live Science in einer E-Mail.
Während die Unterdrückung der Signalübertragung in den Insulin- und TOR-Signalwegen die Lebensdauer von Würmern zu verlängern scheint, ist unklar, ob Menschen die gleiche Reaktion haben würden.
"Wenn das hier identifizierte Gennetzwerk ... bei Säugetieren ähnlich funktioniert, werden pharmakologische Interventionen möglich", sagte Avruch. Mit anderen Worten, die Anti-Aging-Experimente, die zuerst an Würmern durchgeführt wurden, müssen bei Säugetieren wiederholt werden, bevor jemand weiß, ob sie möglicherweise beim Menschen wirken könnten.
Die am Alterungsprozess beteiligten Pfade "könnten etwas sehr Spezifisches für den Wurm sein", sagte Kapahi. "Aber wir werden nie erfahren, ob wir diese Fragen nicht stellen."